Cosa indica 14c?
Sommario
- Cosa indica 14c?
- Quanti isotopi del carbonio esistono?
- Come si forma il c14?
- Cosa sono gli isotopi esempi?
- Quali sono gli isotopi dell'ossigeno?
- Quanti isotopi esistono?
- Quali sono gli isotopi del carbonio e quante particelle contengono?
- Quanti protoni ha il carbonio-14?
- Come avviene la datazione dei fossili?
- What is the most stable isotope of carbon?
- What isotopes of carbon do plants use to make food?
- What is the half-life of carbon radioisotopes?
- How do you find the isotopes of carbon dioxide?
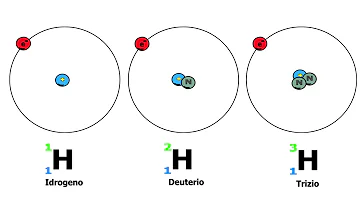
Cosa indica 14c?
Il carbonio-14, 14C (o radiocarbonio) è un isotopo radioattivo del carbonio avente 6 protoni e 8 neutroni. ...
Quanti isotopi del carbonio esistono?
Il carbonio (C) ha 15 isotopi conosciuti, dall'8C al 22C, due dei quali (12C e 13C) sono stabili. Solo tre isotopi (12C, 13C e 14C) possono essere trovati in natura, tutti gli altri sono prodotti artificialmente.
Come si forma il c14?
Il carbonio-14 si forma continuamente nell'alta atmosfera, per effetto dei neutroni dei raggi cosmici sugli atomi di azoto-14. ... Piante ed animali, nel corso della loro vita, assimilano carbonio-14 dall'anidride carbonica.
Cosa sono gli isotopi esempi?
Sono detti isotopi atomi caratterizzati da uno stesso numero atomico (quindi appartenenti a uno stesso elemento) ma aventi numero di massa differente. Gli elementi molto spesso possiedono due o tre isotopi. Per esempio, il carbonio presenta i seguenti isotopi: 612C, 613C, 614 C.
Quali sono gli isotopi dell'ossigeno?
Isotopi. L'ossigeno ha tre isotopi stabili (numero di massa 16, 17 e 18) e dieci radioattivi con emivite molto brevi, inferiori ai tre minuti.
Quanti isotopi esistono?
Gli isotopi sono suddivisi in isotopi stabili (circa 252) e isotopi non stabili o radioattivi (circa 3000 conosciuti ed altri 4000 ipotizzati da calcoli teorici fino l'elemento 118). Il concetto di stabilità non è netto, infatti esistono isotopi "quasi stabili".
Quali sono gli isotopi del carbonio e quante particelle contengono?
Quali sono gli isotopi esistenti in natura del carbonio? I tre isotopi del carbonio sono i nuclidi con con numero di massa 12, 13 e 14. Questi atomi hanno sei protoni ciascuno (e conseguentemente anche sei elettroni) ma differiscono per il numero di neutroni.
Quanti protoni ha il carbonio-14?
6Carbonio-14 / Protoni Come funziona. Il C-14 è un isotopo (atomo) radioattivo del carbonio il cui nucleo è composto da 6 protoni e 8 neutroni (6+8=14): come tutti gli elementi radioattivi è instabile, ossia si trasforma (decade) in un altro elemento perdendo dei protoni.
Come avviene la datazione dei fossili?
Per la datazione di reperti fossili relativamente recenti (di età non superiore a 40 000 anni) si ricorre al metodo del radiocarbonio, con il quale si misura il supporto tra le quantità dei due isotopi del carbonio: il carbonio-14 (14C) radioattivo e il carbonio-12 (12C) stabile.
What is the most stable isotope of carbon?
- Carbon ( 6 C) has 15 known isotopes, from 8 C to 22 C, of which 12C and 13C are stable. The longest-lived radioisotope is 14C, with a half-life of 5,700 years. This is also the only carbon radioisotope found in nature—trace quantities are formed cosmogenically by the reaction 14 N + 1 n → 14 C + 1 H.
What isotopes of carbon do plants use to make food?
- Plants find it easier to use the lighter isotopes ( 12C) when they convert sunlight and carbon dioxide into food. So, for example, large blooms of plankton (free-floating organisms) absorb large amounts of 12C from the oceans.
What is the half-life of carbon radioisotopes?
- This is also the only carbon radioisotope found in nature—trace quantities are formed cosmogenically by the reaction 14N + 1n → 14C + 1H. The most stable artificial radioisotope is 11C, which has a half-life of 20.334 minutes. All other radioisotopes have half-lives under 20 seconds, most less than 200 milliseconds.
How do you find the isotopes of carbon dioxide?
- The quantities of the different isotopes can be measured by mass spectrometry and compared to a standard; the result (e.g. the delta of the 13C = δ13C) is expressed as parts per thousand (‰): Stable carbon isotopes in carbon dioxide are utilized differentially by plants during photosynthesis.















